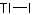
名称:碘化铊
英文名称:Thallium(Ⅰ) Iodide
分子式:
分子量:331.27 g/mol
标签:碘化铊,碘化亚铊,一碘化铊,碘化铊,碘化铊(Ⅰ),碘化铊(I),碘化鉈,Thallous Iodide,Thallium(I) iodide,Thallium iodide (Tl2I2),Thallium iodide (TlI)
编号系统
7790-30-9
MFCD00011279
232-199-7
XG5425000
暂无
24869335
物性数据
1.性状:红色立方体结晶或黄色粉末。[1]
2.熔点(℃):440[2]
3.沸点(℃):824[3]
4.相对密度(水=1):7.1[4]
5.溶解性:微溶于水,不溶于乙醇,溶于王水及浓硫酸。[5]
毒理学数据
1.急性毒性[6]
LD50:24.1mg/kg(大鼠经口);40.7mg/kg(小鼠经口)
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
4.其他有害作用[7] 该物质对环境有危害,应特别注意对水体和空气的污染。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:2
8.表面电荷:0
9.复杂度:2
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.稳定性[8] 稳定
2.禁配物[9] 强氧化剂
3.避免接触的条件[10] 受热、光照
4.聚合危害[11] 不聚合
贮存方法
储存注意事项[12] 储存于阴凉、通风的库房。远离火种、热源。包装密封。应与氧化剂、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
由于TlI在冷水中的溶解度低(例如在10℃时为0.036g/L),把计算量的碘离子(例如KI或HI)加至可溶性的铊盐(例如硫酸盐或高氯酸盐)溶液中可制得TlI。用水洗涤沉淀并在110℃干燥,应在红光下操作以避免光照分解。正如TlCl和TlBr一样,TlI曝光时颜色的改变取决于沉淀的条件。
性质在大约175℃或47×108Pa下TlI发生可逆的结构变化,即从较低对称性的斜方晶型变为亚稳态的红色的8配位数的立方晶型(CsCl结构)。6s和6p能级的混合伴随着铊原子从八面体或立方体场的畸变。对TlI两种晶型的电子光谱和磁化率的估算提出在低温时它的能级混合大约是71%,而在对称性更好的红色立方晶型的能级混合低于28%。
升高温度,TlI将变为更加紧密的CsCl排布,TlI受光照或X射线照射会发光。大约在高于160×108Pa的压力时它表现出金属的导电性。
TlI在稀盐酸和稀硫酸中稳定,但热稀的或冷浓的硝酸能使它分解。在液氨中它与钠反应生成NaTl和NaTl2。人们现已制得TlI与PbI2(3∶1,1∶1),与SbI3(3∶2)和BiI3(2∶1)的复盐。在水溶液中已制得TlI-2,TlI2-3、TlI3-4的碱金属盐和铵盐并已测定了它们的稳定常数。
正如KI+I2可以生成KI3,在减压下蒸发等摩尔的TlI和I2(在浓HI中)溶液可以制备TlI3。X射线数据证明此黑色产物的分子式为Tl+(I-I-I)-。TlI不溶于硫代硫酸钠溶液,也不溶于醋酸铵溶液。
用途
用于制造药物、光谱分析、热定位的特种过滤器、与溴化铊组成混合结晶、传送极长波长的红外辐射。[13]
安全信息
UN 1707 6.1/PG 2
极毒 危害环境
S13 S28 S45 S61
R33 R26/28 R51/53
文献
[1~13]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无





